当前位置:首页 → 职业资格 → 教师资格 → 中学化学学科知识与教学能力->阅读下列材料.按要求完成任务。材料一《普通高中化学课程标准(
阅读下列材料.按要求完成任务。
材料一《普通高中化学课程标准(实验)》关于“氧化还原反应”的内容标准:根据实验事实了解氧化还原反应的本质是电子的转移,举例说明生产、生活中常见的氧化还原反应。
材料二某版本教科书《化学1》的知识结构体系:
第一章从实验学化学
第二章化学物质及其变化
第一节物质的分类
第二节离子反应
第三节氧化还原反应
第三章金属及其化合物
第四章非金属及其化合物
材料三某版本教科书《化学1》第二章第三节“氧化还原反应”片段节选:
请分析下列3个氧化还原反应中各种元素的化合价在反应前后有无变化,讨论氧化还原反应与元素化合价的升降有什么关系。
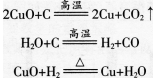
可以看出,在氧化还原反应中,某些元素的化合价在反应前后发生了变化。因此,我们可以说物质所含元素化合价升高的反应是氧化反应,物质所含元素化合价降低的反应是还原反应。
我们再看以下反应:
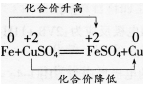
并非只有得氧、失氧的反应才是氧化还原反应,凡是有元素化合物升降的化学反应都是氧化还原反应。
例如.钠与氯气的反应属于金属与非金属的反应。
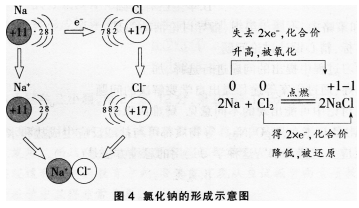
又如.氢气与氯气的反应属于非金属与非金属的反应。从它们的原子结构来看,氢原子的最外电子层上有1个电子,可获得1个电子而形成2个电子的稳定结构。氯原子的最外电子层上有7个电子.也可获得1个电子而形成8个电子的稳定结构。
通过以上分析,我们认识到有电子转移(得失或偏移)的反应,是氧化还原反应。氧化反应表现为被氧化的元素的化合价升高,其实质是该元素的原子失去(或偏离)电子的过程;还原反应表现为被还原的元素的化合价降低,其实质是该元素的原子获得(或偏向)电子的过程。
要求:
(1)氧化还原反应的判断依据是什么实质是什么
(2)确定本节课的三维教学目标。
(3)确定本节课的教学重点和难点。
(4)设计教学思路和教学板书。
(1)氧化还原反应的判断依据是元素的化合价是否发生变化;氧化还原反应的实质是电子的转移(得失和偏移)。 (2)知识与技能目标:能够从化合价升降和电子转移的角度认识氧化还原反应;理解氧化还原反应的本质是电子的转移(得失和偏移),会用化合价的变化和电子转移的观点判断氧化还原反应。
过程与方法目标:通过对氧化还原的特征和本质的分析,学习由表及里以及由特殊到一般的逻辑推理方法。
情感态度与价值观目标:通过对“氧化”和“还原”这一典型矛盾的深入研究,深刻体会自然现象中的对立和
统一的关系,树立辩证唯物主义思想。
(3)重点:从化合价升降和电子转移的角度理解氧化还原反应;了解氧化还原反应的表示方法。
难点:理解氧化还原反应的实质;会用“双线桥”法分析氧化还原反应。

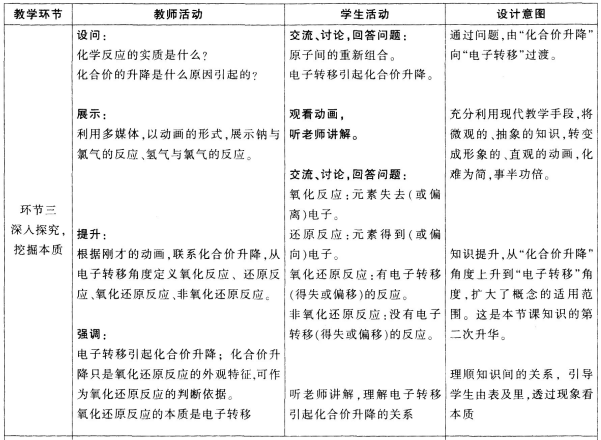

板书设计:
第三节氧化还原反应
一、基本概念:
氧化反应:得氧→化合价升高→失去(或偏离)电子
还原反应:失氧→化合价降低→得到(或偏向)电子
氧化还原反应:得失氧→化合价升降→电子转移(得失或偏移)
二、判断依据:
有元素化合价的变化
三、本质:
电子转移(得失或偏移)
教师职业道德区别于其他职业道德的显著标志就是( )。
教师在直观教学时,应用“变式”方法的目的在于( )。
《普通高中数学课程标准(实验)》提出五种基本能力,没有包含在其中的是
在教学过程中,教师指导学生体验客观事物的真善美的方法是( )。
在学校教育依照特定教学目标组织教学的过程中,起关键作用的是( )。
被毛泽东主席誉为“一代天骄”的成吉思汗( )
"三五步行遍天下,六七人百万雄兵”描写的是( )。
简述学习动机的分类。
简述学生心理发展的基本特征。
在教育史上主张“不愤不启,不悱不发”的教育家是()。