推荐等级:
发布时间: 2021-12-28 16:43
扫码用手机做题
下列有关物质用途的说法错误的是( )
本题解析:
本题考查了物质的用途的知识点。
BaSO4。可用作“钡餐”,是因为既不溶于水又不溶于酸。但BaCO3虽不溶于水,但能溶于酸。其反应的离子方程式为:BaCO3+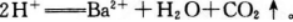
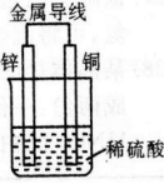
下列关于右图所示装置的叙述,正确的是( )
本题解析:
本题考查了原电池的基本原理的知识点。
如图所示装置为铜、锌原电池,其中铜作正极,铜片上有气泡产生;锌作负极,电流从铜片经导线流向锌片,发生的总反应为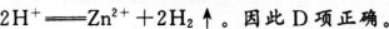
相同浓度的下列溶液,pH值最大的是( )
本题解析:
本题考查了电离、水解对pH的影响的知识点。
①CH3COOH为弱酸,其电离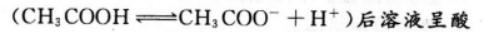 性pH<7;②NaCl为强酸强碱盐,在溶液中不水解,溶液呈中性,pH=7;③NH4Cl为弱碱强酸盐,水解后溶液呈酸性,pH<7;④NaHCO3为强碱弱酸的酸式盐,水解后溶液呈碱性,pH>7。
性pH<7;②NaCl为强酸强碱盐,在溶液中不水解,溶液呈中性,pH=7;③NH4Cl为弱碱强酸盐,水解后溶液呈酸性,pH<7;④NaHCO3为强碱弱酸的酸式盐,水解后溶液呈碱性,pH>7。
下列化合物中,既含有离子键,又含有共价键的是( )
本题解析:
本题考查了离子键与共价键的知识点。
离子键:阴阳离子间通过静电作用所形成的化学键;共价键:原子间通过共用电子对所形成的化学键。本题所给选项H2SO4和CH4都是只含非金属元素,故只存在共价键。KCl中只存在离子键。NaOH中氧原子和氢原子是通过共用电子对(共价键)形成氢氧根,而Na+与OH-又通过离子键结合成离子化合物NaOH,NaOH中既有离子键又有共价键。
下列物质在氧化还原反应中只能作还原剂的是( )
本题解析:
本题考查了氧化荆与还原剂的知识点。
化学反应中失去电子或所含元素化合价升高的物质,为“还原剂”。反之,得到电子或所含元素化合价降低的物质,为“氧化剂”。A项SO2中硫元素的化合价为+4价,其化合价在化学反应中既可以升高(为+6价),也可以降低(为0价或-2价);B项Fe抖中也存在同样的情况,即SO2和Fe2+在氧化还原反应中,既可作氧化剂又可作还原剂;而D项Na+为+1价,在氧化还原反应中只能获得电子被还原,作氧化剂;C项S2-的化合价为-2价,在氧化还原反应中,其化合价只能升高,作还原剂。
把Zn粒加入0.1mol/L盐酸中,若要加快产生H,的速率,可采取的方法是( )
本题解析:
本题考查了影响化学反应的因素的知识点。
滴加少量CuS04溶液后,则发生反应:
下列物质属于纯净物的是( )
本题解析:
本题考查了纯净物和混合物的区别的知识点。
纯净物和混合物的区别在于:前者只有“一种物质”组成,而后者有“多种成分”组成。B项“发烟”硝酸是浓度为98%以上的浓硝酸;C项盐酸是氯化氢气体的水溶液;D项福尔马林则是35%~40%的甲醛水溶液。这三种物质中均含有水,组成成分均不止一种,是混合物。A项小苏打(碳酸氢钠)只由“一种物质”组成,是纯净物。
试卷分类:文科数学
练习次数:0次
试卷分类:历史地理综合
练习次数:0次
试卷分类:理科数学
练习次数:0次
试卷分类:语文
练习次数:0次
试卷分类:语文
练习次数:0次
试卷分类:英语
练习次数:0次
试卷分类:英语
练习次数:0次
试卷分类:物理化学综合
练习次数:0次
试卷分类:物理化学综合
练习次数:0次
试卷分类:物理化学综合
练习次数:0次