122.案例:
下面是两位中学教师关于“酯化反应”的教学过程实录。李老师的教学实录
【播放漫画】看漫画,喝醋能解酒。
【讲述】台州人以豪爽著称,经常以酒会友,为什么喝醋能够解酒
【回答】酸跟醇作用生成酯。
【讲述】同学们回答的很对,大家经过预习已经知道酸跟醇作用生成酯。下面让我们用实验来解释一下这个原理吧。
【活动与探究的讲述】实验的第一步是什么反应所需的药品是什么各起什么作用药品的添加顺序如何浓硫酸的作用是什么得到的反应产物是否纯净主要杂质有哪些如何除去用什么来吸收乙酸乙酯
【实验探究】学生分组讨论,制定实验方案,老师巡回检查,以保证实验安全。
【讲述】像这种酸和醇作用,生成酯和水的反应叫作酯化反应。该反应是可逆反应。
【投影】【思考探究】反应中是乙醇中的C2H5O-取代了乙酸中-OH的位置,还是乙醇中的C2H5-取代了乙酸中H-的位置
【讲述】生物学家们为了研究海豚或某类鱼的活动情况,常采用的方法是将一个跟踪器安装在其身体某部位。同样在化学上我们也可以用一个跟踪器安装在分子里,这种方法称为同位素示踪法。例如将含18O醇与乙酸反应。反应后,18O在乙酸乙酯的位置。证明,乙酸乙酯是乙醇分子中的乙氧基(C2H5O-)取代了乙酸分子中羧基上的羟基(-OH)的生成物。
【课后作业布置】绍兴女儿红非常有名,为什么酒越陈越香,同学们课后想一想
王老师的教学实录
【投影】
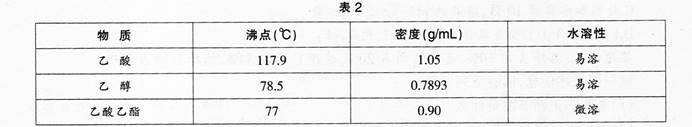
【演示实验】乙酸与乙醇的反应
【讲解】通过实验得出:乙酸与乙醇在有浓硫酸存在并加热的条件可以发生反应,实验中生成的有果香味的无色透明油状液体叫乙酸乙酯。像这种酸跟醇作用生成酯和水的反应叫酯化反应。乙酸与乙醇的酯化反应是可逆的。
【投影思考】
1.为什么导管不插入饱和Na2CO3溶液中
2.反应原理是什么
3.浓硫酸的作用是什么
4.盛饱和Na2CO3溶液的试管中的现象是什么
5.饱和Na2CO3溶液有什么作用
【过渡】在上述这个酯化反应中,生成物水中的氧原子是由乙酸分子中的羧基上的羟基提供还是由乙醇分子的羟基提供如何能证明你的判断是正确的能否提供理论或实验依据
【提问】在酯化反应中乙酸和乙醇有几种可能的断键方式如何确定实际发生的是哪种断键方式
【回答】两种可能的断键情况
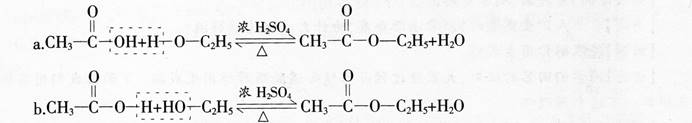
【讲述】用含18O的醇跟羧酸起酯化反应,形成含有18O的酯,证明这种酯化反应的实质是:羧酸脱去羧基上的羟基,醇脱去羟基上的氢原子。
【动画演示】利用同位素原子示踪法验证酯化反应的实质。
【板书】略。
问题:
(1)根据两位老师的教学过程,说明各自所用教学方法的优点。
(2)以李老师的教学为例,说明化学实验对发展学生科学素养具有哪些作用。
(3)根据上述教学实例,归纳总结出化学反应原理这一类知识的基本教学思路。