某短周期元素R,其原子核外最外电子层的电子数比次外电子层的电子数少4个,则其最高价含氧酸的分子式是( )
【解题指要】 (1)“原子核外最外电子层的电子数比次外电子层的电子数少4个”,此句话是本题的关键. 因短周期元素最多只有3个电子层,而此元素至少应有2个电子层——最外层和次外层,所以可能有以下两种情况:
①此元素原子只有2个电子层.因此时,次外层即第一层只有2个电子,所以最外层即第二层不可能比次外层(第一层)少4个电子.故此答案不合理.
②此元素原子有3个电子层.则第二电子层为次外层,其中应有8个电子,最外电子层即第三电子层的电子数为8-4=4个.

(2)根据上述原子的电子层结构,可知该元素位于元素周期表第三周期、第ⅣA族,元素符号为Si,元素名称是硅,最高正化合价为+4价,负化合价为-4价.
由此可推知其最高价含氧酸的分子式是H2SiO3,即为A选项.
把10gMgCl2和MgSO4的混合物溶于适量水中,滴加2mol/L的BaCl2溶液至沉淀完全,共消耗BaCl2溶液25mL。求混合物中MgCl2和MgSO4的质量各是多少克
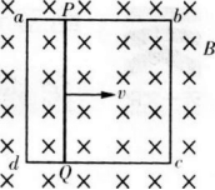
固定在匀强磁场中的正方形导线框abcd,各边长为1.其中ab是一段电阻为R的均匀电阻丝,其余3边均为电阻可忽略的铜线。磁场的磁感应强度为B,方向垂直纸面向里。现有一与ab段的材料、粗细、长度都相同的电阻丝PQ架在导体框上,如图所示。PQ以恒定速度方向如何
一小物块以速度v0=10m/s沿光滑地面滑行,然后沿光滑曲面上升到顶部水平的高台上,并由高台上飞出,如图所示。问当高台的高度h多大时,小物块飞行的水平距离最大这个距离是多少(g=10m/s2)

某晶体盐的水溶液呈浅绿色,在此溶液中通入氯气,溶液变为棕黄色,把所得棕黄色溶液分成两份:一份加入KSCN溶液,溶液变深红色;另一份加入BaCl2溶液,产生不溶于稀HNO3的白色沉淀,则该晶体盐的化学式是_______。
欲除去乙烷中的乙烯,可将混合气体通过盛有_______的洗气瓶;欲除去乙炔中的硫化氢,可将混合气体通过盛有_______的洗气瓶。
浓硝酸常盛装在棕色瓶中,且贮放在冷暗处,原因是_______,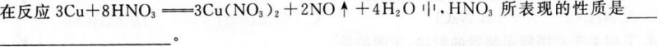
碳酸氢钠溶液和烧碱溶液反应的离子方程式为_______。
常温下,氨水中存在的离子有_______。
在酸或碱存在的条件下,甲酸甲酯跟水发生水解反应的化学方程式为_______。
有下列几种气体:H2、O2、HCl、NO、NH3、CH4,其中通常情况下能用来和水做“喷泉”实验的是_______。