金属历来都是通过采矿、冶金制取的。可是20世纪80年代初期,科学家发现在聚乙炔中加入强氧化剂或还原剂后,它的导电性能大大提高。因为这种塑料具有金属的一般特性,所以人们称它为“人造金属”。近年来,它的发展极为神速,人们又先后研制成功了聚苯乙炔、聚苯硫醚和聚双炔类等。这种“人造金属”不仅具有金属光泽,还能导电传热,其用途十分引人瞩目。
“人造金属”最奇特的功能就是它的导电性。与普通塑料不同的是,“人造金属”塑料具有一种独特的线性结构,许多同样的分子能奇妙地结合起来,并带来较多的“自由”电子,这就使原来的塑料改变了物理性能,能够导电。它的导电率比铜、银还要高。普通金属的导电性随着温度的降低而增大,在接近绝对零度时成为超导,但这种低温很难得到。而人造金属却相反,随着温度升高,外围“自由”电子释放越来越多,因而导电性增大,在常温下就呈现出超导电性能。实现超导,由低温变成常温,这是“人造金属”创造的一大奇迹,是科学家梦寐以求的目标,用超导体制造的发电机,它的效率可以从30%提高到 98%,超导电线将使远距离无损耗输电的设想成为可能,使火车悬浮在轨道上高速运行,并将使有控热核聚变反应成为现实,最终解决能源的问题。 “人造金属”的另一突出贡献是,用它制成新型电池代替笨重硕大的铅蓄电池,可以使A&q长期盼望的用蓄电池做动力的汽车有了实现的可能。“人造金属”电池可提供相当常规电池l0倍的电力,不需要维修,充电次数可达1000次以上,使用寿命比铅蓄电池长4~5倍,而且不会污染环境。
“人造金属”在外压和光的作用下,都能产生电场效应,把它装在扩音器上,能将声音放大;把它装在红外摄像机上,在红外热能作用下,也能产生工作电流进行录像。此外,“人造金属”塑性大,易加工,重量轻,耐磨蚀性能好,强度大,成本低。
对“人造金属”导电性的判断,正确的一项是( )
把10gMgCl2和MgSO4的混合物溶于适量水中,滴加2mol/L的BaCl2溶液至沉淀完全,共消耗BaCl2溶液25mL。求混合物中MgCl2和MgSO4的质量各是多少克
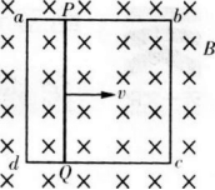
固定在匀强磁场中的正方形导线框abcd,各边长为1.其中ab是一段电阻为R的均匀电阻丝,其余3边均为电阻可忽略的铜线。磁场的磁感应强度为B,方向垂直纸面向里。现有一与ab段的材料、粗细、长度都相同的电阻丝PQ架在导体框上,如图所示。PQ以恒定速度方向如何
一小物块以速度v0=10m/s沿光滑地面滑行,然后沿光滑曲面上升到顶部水平的高台上,并由高台上飞出,如图所示。问当高台的高度h多大时,小物块飞行的水平距离最大这个距离是多少(g=10m/s2)

某晶体盐的水溶液呈浅绿色,在此溶液中通入氯气,溶液变为棕黄色,把所得棕黄色溶液分成两份:一份加入KSCN溶液,溶液变深红色;另一份加入BaCl2溶液,产生不溶于稀HNO3的白色沉淀,则该晶体盐的化学式是_______。
欲除去乙烷中的乙烯,可将混合气体通过盛有_______的洗气瓶;欲除去乙炔中的硫化氢,可将混合气体通过盛有_______的洗气瓶。
浓硝酸常盛装在棕色瓶中,且贮放在冷暗处,原因是_______,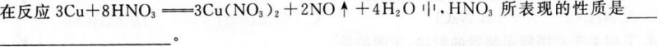
碳酸氢钠溶液和烧碱溶液反应的离子方程式为_______。
常温下,氨水中存在的离子有_______。
在酸或碱存在的条件下,甲酸甲酯跟水发生水解反应的化学方程式为_______。
有下列几种气体:H2、O2、HCl、NO、NH3、CH4,其中通常情况下能用来和水做“喷泉”实验的是_______。